
ES&T | 微塑料的生物老化及促炎新机制
近年来随着微塑料在人体中被检测到的证据越来越多,微塑料的健康风险也备受关注。然而已报道的相关研究多聚焦于微塑料原始状态的健康风险,或是致力于模拟微塑料在环境介质中的老化过程及其环境老化后的毒理学效应。对微塑料进入机体后长期滞留引发的“生物老化”特征及其毒理学效应仍缺乏系统认识。
12月30日,中国科学院深圳先进技术研究院李洋研究员团队在Environmental Science & Technology发表研究论文,系统分析了微塑料在体内长期滞留过程中的“生物老化”理化表征变化,阐明生物老化过程能够增强微塑料与关键炎症信号分子相互作用,赋予微塑料“特洛伊木马”功能,进而激活非典型炎症信号通路,放大炎症反应,最终加重机体炎症病理。该研究为阐明微塑料体内长期命运与其健康风险机制之间的内在联系提供了重要证据。
以往关于微塑料老化的认知,主要集中于其在自然环境中所经历的光氧化、热降解等过程,即“环境老化”。然而,当微塑料通过摄入等途径进入人体后,由于其稳定的化学性质,难以被生物降解,部分可能长期滞留于组织内。在体内生理环境下,微塑料可能经历持续数年的“生物老化”过程。然而生物老化对微塑料颗粒性质的影响,以及生物老化微塑料所引发的生物学效应,长期以来一直是一个尚未揭示的科学黑箱。另一方面,现有毒理学研究较多关注微塑料浸出液或其负载重金属等化学物质后的毒性,却忽视了微塑料与胃肠道等复杂生理环境中丰富的生物活性分子之间可能发生的特异性相互作用。值得注意的是,此类相互作用恰恰可能主导微塑料的长期健康风险。在肠腔及炎症相关微环境中,脂多糖(LPS)作为革兰氏阴性菌细胞外膜的关键成分,属于病原体相关分子模式(PAMP),在肠屏障受损或菌群失衡等情况下更容易触发宿主的炎症反应。因此,探究生物老化微塑料与LPS的相互作用具有明确的生理学意义。
基于此,本研究旨在系统探究微塑料在体内生理环境中的长期生物老化效应。研究团队利用在胃肠模拟液环境中生物老化12个月的聚苯乙烯微塑料,首次直接观察并检测其生物老化过程中的理化表征变化。结果显示,长期体内环境暴露会深刻重塑微塑料表面,使其发生氧化、亲水性增强,尤其是表面粗糙度显著提升。这些界面理化性质的改变,预示着其与生物分子相互作用能力可能发生根本性变化。为精确量化生物老化微塑料与LPS的相互作用,本研究基于生物力学检测,联合原子力显微镜、分子动力学模拟及生物层干涉技术等多种手段证实,生物老化后增加的表面粗糙度,显著增加微塑料与LPS之间的结合力。并且这种增强效果使老化微塑料能够更大量且稳定地吸附LPS,在其表面形成更厚且致密的“LPS冠层”,使其从惰性颗粒转变为搭载促炎分子的“特洛伊木马”。当这些负载厚重LPS冠的老化微塑料被巨噬细胞识别并摄取后,微塑料载体可将LPS递送至细胞质内部。这一过程使得LPS绕过了传统细胞膜Toll样受体4介导的识别路径,在胞内直接被炎症蛋白酶caspase-11识别,进而激活非经典炎症小体通路:切割激活Gasdermin D并在细胞膜上形成孔道导致细胞焦亡;协同激活经典NLRP3炎症小体,促进caspase-1对白细胞介素-1β前体的切割与成熟,成熟IL-1β经Gasdermin D孔道大量释放到细胞外,最终放大炎症反应。
进一步,研究团队选取葡聚糖硫酸钠(DSS)诱导的小鼠结肠炎模型,对生物老化微塑料负载LPS所产生的“特洛伊木马效应”及其在肠道炎症中的影响进行了检测。结果显示,口服负载LPS的生物老化微塑料显著加剧了疾病严重程度,表现为更明显的体重下降、结肠长度缩短及肠道屏障损伤加重。这些结果进一步证实,生物老化微塑料作为一种相对惰性的载体,可在肠道中吸附并携带LPS等强促炎因子。当负载LPS的生物老化微塑料被巨噬细胞摄取后,可将原本不易进入细胞的毒素“搭载”至胞内,从而增强细胞内炎症信号的激活与放大,最终加剧炎症反应并阻碍组织修复。
本研究首次完整揭示了微塑料在生理环境中的长期生物老化过程,及其对颗粒界面性质与炎症信号传递能力的重塑作用。生物老化改变了微塑料的表面特性,使其从相对“惰性颗粒”转变为能够“携带并递送促炎信号”的载体。载体被巨噬细胞摄取后,可将表面结合的促炎分子转移至细胞内部,从而在细胞内触发并放大免疫反应,最终加剧炎症并扩展组织损伤。
本研究从环境毒理学角度阐明:颗粒物的健康风险并非仅由其初始理化性质决定。进入生物体后,颗粒经历“生物老化”后,经过表界面性质重塑,与生理环境中的生物分子互作后,被赋予新的功能。在此过程中,一些原本低毒或无毒的微塑料,因获得携带促炎分子、增强细胞内信号传递的能力,转变为具有更高生物危害的“载毒复合体”,产生“特洛伊木马效应”。
本研究通讯作者为中国科学院深圳先进技术研究院(SIAT)李洋研究员,张国芳副研究员,河北科技大学王英泽教授,河北师范大学常彦忠教授。巴塞罗那自治大学-SIAT联培博士生李奇,SIAT王晓峰工程师,河北师范大学-SIAT联培已毕业硕士徐雅晴为共同第一作者。研究工作得到了科技部重点研发计划、国家自然科学基金、广东省自然科学基金等项目的资助,并得到了西班牙加泰罗尼亚纳米科学与纳米技术研究所Victor F. Puntes教授团队的帮助。
本研究从微塑料—生物分子互作出发,阐明生物老化能够增加微塑料的表面粗糙程度,改变其表界面性质,从而增强其与生物分子互作,最终揭示其免疫毒理学效应的分子机制。李洋研究员团队长期围绕纳米颗粒与生物分子相互作用开展系统研究,致力于解析纳米-生物分子互作规律及机制解析,阐明纳米颗粒生物学效应的分子机制,为评估纳米颗粒的毒理学效应机制或开发纳米分子靶向药物,提供全新的理论基础和研究范式。相关研究发表于Nature Nanotechnology,Journal of the American Chemical Society,Advanced Functional Materials等期刊。

原文链接:https://pubs.acs.org/doi/10.1021/acs.est.5c12882
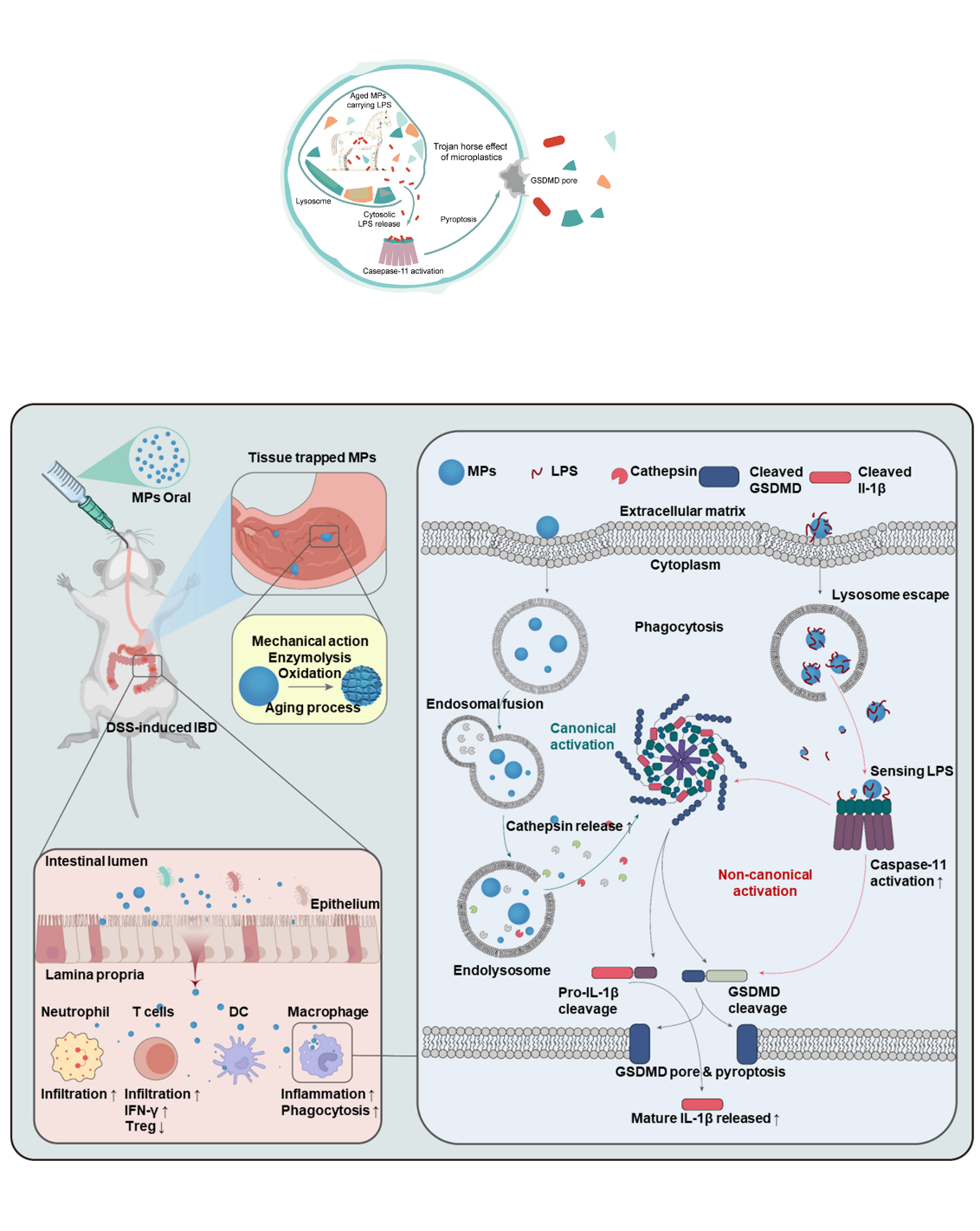
图1. 生物老化微塑料携带脂多糖进入巨噬细胞并放大炎症反应的“特洛伊木马效应”机制
附件下载: