
Nature Communications | CPPTACs介导的细胞膜蛋白靶向降解
细胞膜蛋白作为药物研发的核心靶点,其重要性已被大量临床药物证实。细胞膜蛋白靶向降解技术能选择性清除致病蛋白,展现出更强治疗潜力,开辟了药物研发的新范式。
近日,由中国科学院深圳先进技术研究院医药所房丽晶研究员、陈亮副研究员与李红昌研究员组成的学科交叉团队,在细胞膜蛋白靶向降解技术方面取得重要进展。该团队成功开发出一种新型穿膜肽介导的膜蛋白靶向降解技术——CPPTACs。该技术利用穿膜肽(CPPs)诱导的内吞作用,在不依赖溶酶体转运受体的情况下,成功实现了疾病相关膜蛋白的高效特异性降解,具有结构简洁、治疗窗口宽、适用性广等优势,为靶向膜蛋白降解提供了普适性解决方案。该成果以“Targeted Degradation of Cell Surface Proteins through Endocytosis Triggered by Cell-Penetrating Peptide-Small Molecule Conjugates”为题发表于国际学术期刊《自然·通讯》(Nature Communications)。
近年来兴起的以LYTACs为代表的多种膜蛋白靶向降解技术,利用双功能分子在细胞膜表面桥接靶蛋白与特定溶酶体转运受体(LTR),以借助LTR的内吞作用将靶蛋白转运至溶酶体降解。然而,此类技术的降解效率和适用范围受限于LTRs的活性和表达水平,且“绑架”这些功能受体可能引发潜在副作用。因此,开发不依赖特定受体、适用性更广的膜蛋白降解技术成为迫切需求。
针对上述问题,研究团队创新性地开发了一种基于穿膜肽(CPP)的膜蛋白靶向降解策略—CPPTACs(CPP-mediated lysosome-targeting chimeras)。CPPTAC降解剂由一个穿膜肽与一种靶蛋白(POI)配体偶联得到,能够通过多种不同的CPP驱动细胞膜和胞外POI的內吞,并将其运输到溶酶体中进行降解。在细胞水平,CPPTACs能够高效降解PD-L1、CAIX以及CB2R等多种疾病相关的膜蛋白。在动物模型中,CPPTAC也能够诱导靶标蛋白(PD-L1)降解,并且在小鼠模型中表现出显著的肿瘤抑制作用和低毒副作用。团队进一步采用CRISPR knockout library和竞争性抑制实验研究了影响CPPTACs作用的关键因素。研究表明,CPPTACs的作用机制依赖于其正电荷与细胞膜上蛋白聚糖负电荷之间的静电相互作用,而非通过单一的溶酶体转运受体。该机制克服了现有靶向降解技术对特定受体的依赖性,为细胞膜蛋白的靶向降解提供了一种简单且通用的策略,在化学生物学和药物化学领域具有重要应用潜力。
深圳先进院研究助理何婉仪,陈从丽,郑纪维和博士后李艳艳为该论文的共同第一作者;房丽晶研究员、陈亮副研究员和李红昌研究员为论文共同通讯作者。该研究得到了国家重点研发计划、广东省自然科学基金、深圳市医学科学院和深圳市科技创新局项目的资助。

文章上线截图https://www.nature.com/articles/s41467-025-62776-w
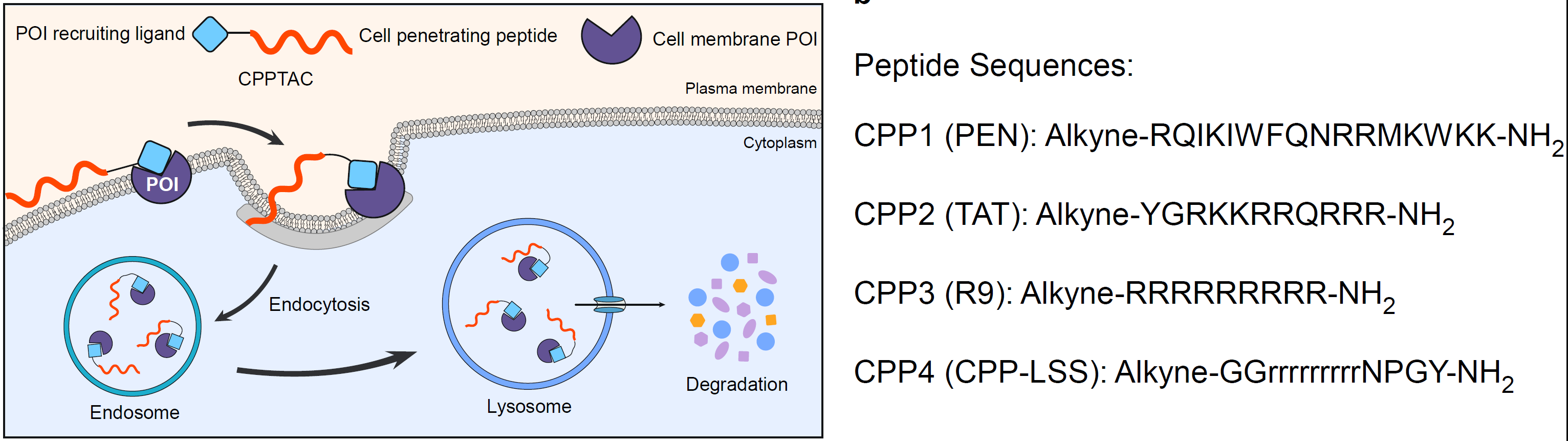
CPPTACs降解剂的构建原理和作用模式图
附件下载: